Exossomo
Exossomos são um subtipo de vesículas extracelulares, estruturas fechadas de bicamada lipídica derivadas de células e secretadas por quase todos os tipos de células, incluindo exossomos (30-150 nm), microvesículas (150 nm a 1 μm) e corpos apoptóticos (1-5 μm). Há muito tempo acredita-se que essas vesículas sejam uma forma de transportar os resíduos produzidos pela célula. Foi somente na década de 1980, quando pesquisadores estudavam o desenvolvimento de reticulócitos de ovelha, que eles inicialmente determinaram o papel de algumas vesículas de 30-150 nm e as denominaram exossomos. Observados ao microscópio eletrônico, os exossomos geralmente têm formato de copo ou esférico. Eles protegem e transportam macromoléculas funcionais, incluindo ácidos nucleicos, proteínas, lipídios e carboidratos, entre as células e transferem suas “cargas” para as células receptoras.
Com base em anos de pesquisa, a indústria reconheceu o potencial dos exossomos em uma variedade de aplicações. Em ensaios clínicos atuais, exossomos são utilizados como biomarcadores, terapias livres de células (terapia com exossomos), sistemas de liberação de fármacos e vacinas antitumorais. Suas fontes incluem células mesenquimais, células T e células dendríticas, bem como outras linhagens celulares modificadas.
Os exossomos apresentam vantagens insubstituíveis, como vetores de liberação de fármacos, incluindo baixa imunogenicidade, excelente biocompatibilidade e bioestabilidade. Além do uso de exossomos naturais sem qualquer modificação genética/química, existem duas maneiras principais de carregar cargas úteis em exossomos: no método direto, os exossomos são carregados com fármacos terapêuticos após a purificação (carregamento exógeno), enquanto no método indireto, células apropriadas são geneticamente modificadas ou cocultivadas com fármacos terapêuticos para produzir exossomos modificados (carregamento endógeno).
Para carga exógena, a indústria tem explorado várias estratégias para carregar fármacos em exossomos e maximizar seu potencial de entrega, incluindo incubação simples, bem como eletroporação, sonicação, congelamento-degelo, etc. Geralmente, há algumas diferenças entre os estudos, atribuídas ao comportamento biológico de diferentes células parentais e propriedades dos reagentes. Além disso, os exossomos são naturalmente carregados com proteínas e ácidos nucleicos naturais, o que reduz significativamente a eficiência de carga necessária. O método correto para atingir a carga ideal depende, em certa medida, da molécula de carga, que deve ser cuidadosamente selecionada com antecedência e deve considerar a capacidade de carga, a retenção do fármaco e os efeitos potenciais nas propriedades do exossomo. As limitações das estratégias de carga direta limitam o uso de terapias baseadas em exossomos em ensaios clínicos.
A criação e o uso de exossomos projetados e projetados de forma racional e proposital, com propriedades altamente definidas e reprodutíveis e um mecanismo de ação conhecido, constituem uma alternativa atraente aos exossomos de origem natural, que frequentemente são altamente heterogêneos e possuem mecanismos de ação pouco claros, além de serem uma base mais viável para o desenvolvimento de novos fármacos importantes. No entanto, as abordagens de engenharia exigem certas melhorias na manutenção das propriedades físico-químicas ideais dos exossomos e na melhoria da eficiência de carregamento. Outro desafio é que a maioria dos métodos utilizados para a engenharia de exossomos tem dificuldade em encontrar um equilíbrio entre o carregamento estável da carga desejada e a modificação da superfície versus a manutenção da biocompatibilidade do exossomo.
Outro gargalo na expansão de terapias baseadas em exossomos para produção em escala industrial e, posteriormente, para ensaios clínicos é a produção de exossomos de grau clínico em larga escala. O rendimento dos exossomos é altamente dependente de suas células-mãe, limitado pelas diferentes capacidades das células de secretar exossomos e pela alta dificuldade e custo da cultura celular em larga escala. Para a aplicação farmacêutica de exossomos, a expansão para níveis industriais ainda está em fase inicial, sendo de suma importância determinar os métodos que possam produzir o número necessário de exossomos contendo cargas terapêuticas o mais rápido possível.
A ineficiência dos métodos de isolamento de exossomos em larga escala é outro obstáculo ao desenvolvimento de exossomos de nível clínico. A quantidade, as características físico-químicas e a composição dos exossomos liberados por diferentes tipos de células podem variar. Atualmente, tecnologias baseadas em diferentes princípios têm sido utilizadas para o isolamento de exossomos, incluindo ultracentrifugação diferencial/ultracentrifugação, filtração, cromatografia de exclusão por tamanho, captura baseada em imunoafinidade, precipitação, etc. Embora alguns métodos de purificação de exossomos tenham sido desenvolvidos e otimizados, ainda é difícil encontrar um método específico que solucione todos os desafios relacionados, como baixa eficiência de separação, perda de amostra, baixa recuperação e pureza do exossomo e variabilidade entre lotes. Portanto, também é crucial caracterizar completamente os exossomos, especialmente em termos de tamanho, morfologia, concentração, presença de marcadores/conteúdos exossômicos e remoção de contaminantes.
Métodos de isolamento de exossomos comumente utilizados e suas vantagens e desvantagens
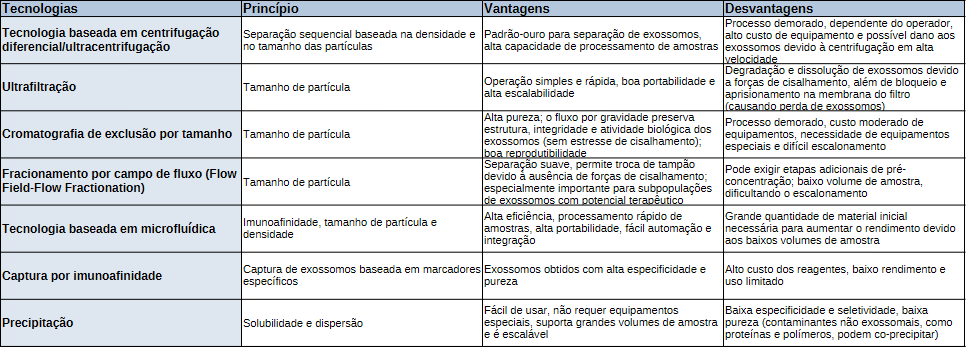
Embora ainda existam desafios e limitações, diversas empresas farmacêuticas e startups abriram caminho para o desenvolvimento de terapias com exossomos de nível clínico. Um número crescente de empresas está se concentrando no desenvolvimento de terapias baseadas em exossomos para abordar problemas de administração de fármacos em uma variedade de terapias, incluindo pequenas moléculas, terapias de RNA, proteínas, terapias gênicas virais e até mesmo ferramentas de edição gênica por repetições palindrômicas curtas regularmente interespaçadas (CRISPR). Algumas dessas empresas também estão buscando métodos mais inovadores de engenharia de exossomos para projetar terapias baseadas em exossomos, a fim de aumentar a carga do fármaco e melhorar a capacidade de direcionamento.
Os métodos tradicionais de administração de RNA, proteínas e moléculas químicas têm apresentado algumas limitações, enquanto os exossomos como vetores de administração de fármacos apresentam grandes vantagens, como baixa imunogenicidade, segurança a longo prazo e ausência de citotoxicidade. Ainda existem desafios a serem superados na tradução clínica, produção em larga escala, preparação estável, estratégias de armazenamento e controle de qualidade de fármacos baseados em exossomos. O desenvolvimento adicional de exossomos projetados a partir de células e suas tecnologias de separação, purificação e carregamento de fármacos ajudará a superar essas deficiências. Os exossomos projetados apresentam vantagens comerciais significativas no aumento da produtividade. Além disso, ao ancorar moléculas de superfície específicas aos exossomos, a concentração local de exossomos nas células ou tecidos-alvo pode ser aumentada, reduzindo assim a toxicidade e as reações adversas e maximizando os efeitos terapêuticos. No futuro, a indústria provavelmente desenvolverá novos exossomos multifuncionais projetados para aprimorar a assistência médica, portanto, mais pesquisas são necessárias para explorar novas estratégias para terapias mediadas por exossomos.
A Duoning Biotech está comprometida em ser uma fornecedora completa de tecnologia de bioprocessos para atender a todas as necessidades específicas de diversas terapias emergentes em diferentes estágios, a fim de ajudar mais produtos terapêuticos a passar da pesquisa para os ensaios clínicos e, finalmente, para a comercialização.


