Vírus Oncolítico (Oncolytic Virus - OV)
Os Vírus Oncolíticos (OVs) são considerados particularmente promissores porque têm dois modos de ação principais: eles podem matar células tumorais infectadas e estimular a imunidade antitumoral para promover o desenvolvimento de imunidade antitumoral contra células tumorais não infectadas. Além disso, existem outros efeitos associados. Por causa disso, eles oferecem a possibilidade de aprimorar significativamente as terapias tumorais existentes. No entanto, o histórico de sucesso comercial associado à terapia com Vírus Oncolíticos é relativamente curto. Embora algumas terapias com Vírus Oncolíticos à base de Adenovírus tenham sido aprovadas por agências reguladoras na China e em outros países anteriormente, a primeira a obter a aprovação do FDA e da EMA e causar o foco mais amplo da indústria em terapias oncolíticas veio em 2015 com o Talimogene Laherparepvec (T-VEC) da Amgen, um Vírus Oncolítico HSV-1 recombinante, e a aprovação mais recente foi o Teserpaturev da Daiichi Sankyo. ou G47Δ (DELYTACT®), também uma forma modificada do HSV-1, recebeu aprovação condicional e por tempo limitado no Japão para glioblastoma em junho de 2021.
Embora a comercialização bem-sucedida de Vírus Oncolíticos como imunoterapias seja relativamente nova, a ciência por trás deles tem uma longa história, desde que os cientistas observaram pela primeira vez a progressão tumoral lenta em alguns pacientes com infecções virais e microbianas vivas. Pesquisadores já começaram a explorar vírus como ferramentas anticâncer. Nas últimas décadas, essa observação de patógenos naturais foi aplicada a uma variedade de vírus projetados, incluindo HSV-1, Adenovírus, Poliovírus, Vírus do Sarampo e outros. A compreensão de como esses vírus funcionam também está melhorando constantemente. Além dos produtos aprovados, muitas Terapias Oncolíticas Virais desenvolvidas utilizando diversas plataformas virais estão atualmente em ensaios clínicos, muitos dos quais têm mostrado resultados promissores.
A pesquisa atual sobre o design de Vírus Oncolíticos tem se concentrado em adicionar a Vírus Oncolíticos com vários transgenes para aumentar sua estimulação imunológica, modular pontos de controle imunológicos e fornecer alvos de imagem. Ao se esforçar para sinergizar Vírus Oncolíticos com outros Imunomoduladores ou Agentes Citotóxicos, os desenvolvedores esperam alcançar a imunoterapia tumoral mais eficaz. Embora os pesquisadores continuem a otimizar esses vírus e sua produção por meio de diversas estratégias de engenharia viral, muitos objetivos relacionados à segurança, eficácia e escala comercial desses produtos estão desafiando seu caminho, incluindo como atingir alto rendimento viral, atributos críticos de qualidade altamente reprodutíveis, estabilidade genética e estabilidade da formulação e do produto.
Um desafio que está retardando o desenvolvimento dessas terapias é garantir a relativa segurança dos Vetores Virais. A maioria dos Vírus Oncolíticos se replica condicional ou parcialmente, principalmente em células tumorais, e minimizar a possibilidade de replicação viral em células saudáveis é uma consideração primordial nos ensaios clínicos iniciais. Esse aumento na segurança destaca a importância dos estágios iniciais do design de Vetores Virais, desde a seleção da linhagem celular até a otimização da infecção. Para Bioterapêuticos que podem se replicar, mesmo aqueles restritos a tipos específicos de células ou estágios do ciclo celular, garantir que o vírus não possa retornar à competência total de replicação é essencial para o avanço da terapêutica no processo de desenvolvimento.
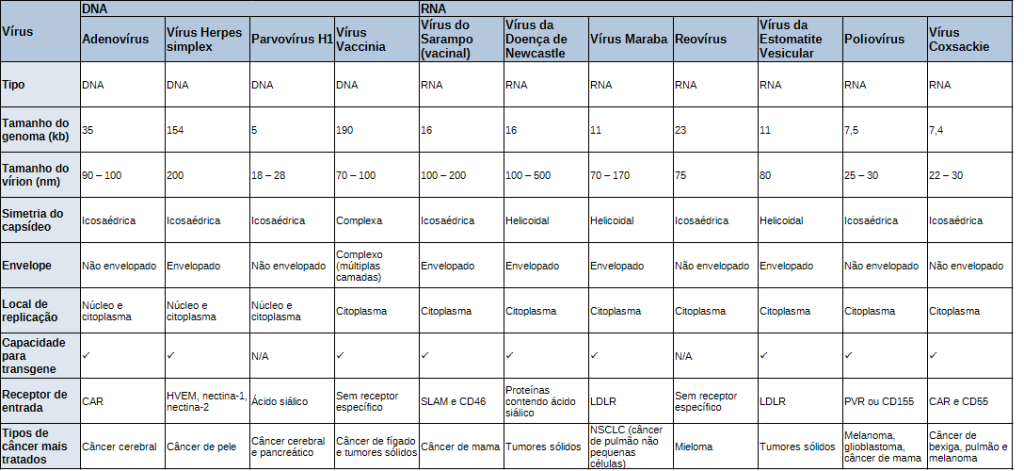
O design e a engenharia de vetores, em conjunto com outros aspectos do desenvolvimento inicial do produto, são essenciais para reduzir a possibilidade de replicação ou expressão de células fora do alvo após a administração de um medicamento a um paciente. O design adequado do vetor é fundamental. Vetores projetados incorretamente ou o uso de linhagens celulares não otimizadas podem levar à instabilidade genética, incluindo o potencial de produzir vírus totalmente replicativos, bem como o potencial de produzir variantes ou subtipos transgênicos que afetam a eficácia e a segurança viral. Da mesma forma, o impacto da seleção da linhagem celular, do tipo de cultura, do meio, dos suplementos, da otimização da infecção e dos processos iniciais de coleta a jusante no rendimento e na pureza do vírus requer uma abordagem integrada e multifacetada. Em particular, a escolha do meio utilizado para o cultivo das células não deve afetar sua segurança e produtividade, de modo que a seleção do meio se torna uma parte importante para garantir o escalonamento ideal.
Além disso, devido às diferenças significativas entre os diferentes vírus oncolíticos, é necessário projetar um processo de produção direcionado de acordo com as características de cada vírus. Em geral, no entanto, o processo de produção viral começa com a seleção da linhagem celular de produção, incluindo o crescimento em cultura aderente ou em suspensão, lise celular, otimização do meio e do tampão, purificação viral e produção asséptica, sendo esta última especialmente importante para vírus com partículas maiores. Vírus, como o da vacina, não podem ser filtrados estéreis pelas mesmas etapas que os adenovírus e outros vírus pequenos não envelopados. Assim como acontece com outros produtos baseados em vetores virais, as instalações de fabricação exigem o mais alto nível de comprometimento com a conformidade com as BPF e a esterilidade, empregando tecnologias de uso único e até mesmo sistemas fechados sempre que possível para evitar qualquer potencial contaminação cruzada.
Além disso, como mencionado anteriormente, como existem atualmente no mercado apenas algumas terapias virais oncolíticas aprovadas, o ambiente regulatório que as envolve permanece relativamente fluido, e o desenvolvimento de vetores virais oncolíticos requer atenção aos requisitos regulatórios em constante mudança aplicáveis a essas terapias. Como cada vírus usado em aplicações virais oncolíticas possui características únicas, podem surgir caminhos de aprovação exclusivos, específicos para diferentes produtos virais oncolíticos, com base no vírus escolhido e no modo de ação. Ao mesmo tempo, embora os vetores virais testados para aplicações de vacinas e oncolíticos sejam amplamente consistentes, há algumas diferenças importantes: normalmente, os vírus oncolíticos têm componentes recombinantes ativos adicionais, geralmente imunomoduladores, e, portanto, exigem testes mais aprofundados, ou seja, a confirmação da eficácia e segurança dos produtos virais oncolíticos pode exigir novas estratégias de testes analíticos.


